
23.【答案】(1)左(1分)右(1分)(2)①17.5(17.3~17.7均可)(1分)U②如图所示(2分)③直线(1分)一(1分)5.0(2分)【关键能力】本题通过探究影响感应电流方向的因素、变压器原、副线圊电压与匝数的关系,考查考生的理解能力、信息加工能力、实验探究能力。【学科素养】本题考查的学科素养是科学探究和科学思维,要求考生能通过所学电磁感应和电学实验知识分析试题,并能熟练利用图象法处理实验数据。【解题思路】(1)对调电源正负极,闭合开关,感应电流方向将会反向所以G1指针向左偏转;又改变A线圈的绕行方向,闭合开关,感应电流再次反向,电流自下而上流入C2,所以G2将向右偏转。(2)①表盘每一小格表示1V估读一位,所以为17.5V(173V~17.7V);②描点、连线如图所示;③图线显然为直线且过原点n,由。1U可知,U. n图线斜率倒数为U4=50V。


28.【答案】(1)将旧铍铜元件粉碎、适当提高反应温度(2分,合理即可)CuS、FeS(2分)H2SiO3(或HSi04,2分)(2)BeO 20H=Be02 H20(2分)(3)加入过量的氨水生成Be(OH):,过滤、洗涤后再加入盐酸,可得到BeCl2溶液最后在HC气流中蒸发结晶可以得到BeCl固体(2分,合理即可)(4)MnO, CuS 2H. SO, = MnS0 $ CuSO, 2H, 0(2 4)(5)4(2分)【关键能力】本题考查的关键能力侧重于分析与推测、探究与创新能力。【必备知识】本题考查的必备知识包括工艺流程分析、反应条件的控制、元素化合物的性质、方程式的书写、物质的分离等。【解题思路】(1)旧铍铜元件加人过量的氢氧化钠溶液,可以采取将旧铍铜元件粉碎、适当提高反应温度、提高氢氧化钠溶液的浓度等措施提高旧铍铜元件的浸取率。(2)根据题意可知铍、铝元素的化学性质相似,BeO可以和NaOH溶液发生反应:BeO 2OH=BeO2H2O。(3)旧日铍铜元件溶于NaOH溶液生成Na2BeO2,且SiO2也可以和NaOH溶液反应生成Na2Si0O3,所以滤液A含有NaOH、Na2SiO3、Na2BeO2等,滤液A中加入过量HCl得到的固体C应为H2SiO3沉淀,滤液C中则主要含BeCl2、NaC和HCl,为提纯BeCl2,可先加入过量的氨水生成Be(OH)2,过滤、洗涤后再加入盐酸,可得到BeCl2溶液,最后在HCl气流中蒸发结晶可以得到BeCl2固体。(4)滤渣B中含有CuSFeS,加入二氧化锰、稀硫酸发生氧化还原反应,根据题意可知酸性环境中MnO2能将金属硫化物中的硫元素氧化为硫单质,与CuS反应,还可生成硫酸铜、硫酸锰,结合元素守恒和得失电子守恒可得反应的化学方程式为MnO2 CuS 2H2SO4=MnSO4 S CuSO4 2H2O。K。[Cu(OH)2(5)常温下,当铜离子开始沉淀时,c(OH)=√c(Cu2)2.2×105√2.2mlL=1xl0"ml·L,此时pH=4,所以p应大于4

以上就是英语周报2022九年级外研覅答案,更多英语周报答案请关注本网站。

 相关文章
相关文章



 栏目最新
栏目最新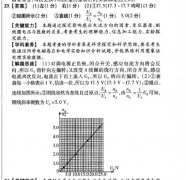

 随机推荐
随机推荐 热门标签
热门标签