


19.(14分)(1)①<(1分)②C>B>A(1分)③CN CO2 H2O一HCN HCO(2分)④CH;COO H2OCH2COOH OH(1分)1.8×104(1分)(2)9:1(2分)(3)①c(C-》>c(NH)>c(H )>c(OH-)(2分)②2×10-5-2×10-(2分)(4)HSO(1分)1.91(1分)【解析】(1)①根据表中数据可知,酸性:HCN H2CO3>HCN>HCO3。酸越弱,对应的酸根离子越易水解,故溶液的pH由大到小的顺序为C>B>A③酸性:H2CO3>HCN>HCO,故反应的离子方程式为CN- CO2 H2OHCN HCO。④ CH, COONa是强碱弱酸盐,CH3COO-水解导致溶液呈碱性;c(CH, Co0-) K (CH, COOH)c(CH, COcc(H )1.8×10-510=1.8×10(2)由题意可知,该温度下,K。=10-1。pH=11的NaOH溶液中c(OH)=0.1molL-1,pH=2的H2SO4溶液中c(H )=0.01mol・L-1,混合后pH变为9。设H2SO4溶液的体积为V1L,NaOH溶液的体积为vL,则10~9.1v=0,解得v=9:1。3)①d点为氯化铵溶液,溶液中c(Cl-)>c(NH)>c(H )>c(OH)。②b点为等浓度NHC和NH,・H2O的合溶液,根据电荷守恒和物料守恒得,2c(Hc(NH )=2c(OH-) c(NH3・H2O),则c(NH )c(NH3・H2O)=2c(OH-)-2c(H )=(2×10-5-2×10-)mol・L-1(4)溶液中含S的微粒有H1SO、HSO、9O,由图可知,该微粒为HSO5。K。t=c(H )・c(HSO)c(H2sO)1.91时,含HSO万的物质的量分数为50%,此时可近似认为c(H2SO3)=c(HSO),则Ks≈c(H )=10-1n,pKa=-lgK,≈1.91。
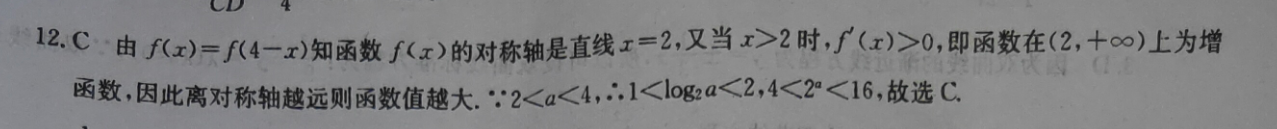
12.C由f(x)=f(4-x)知函数f(x)的对称轴是直线x=2,又当x>2时,(x)>0,即函数在(2, ∞)上为增函数,因此离对称轴越远则函数值越大∵2

以上就是2022高二课标英语周报第8期答案,更多英语周报答案请关注本网站。





 相关文章
相关文章


 栏目最新
栏目最新

 随机推荐
随机推荐 热门标签
热门标签