

21.向预测……解析几何是全国卷的必考内容,常以解答题的形式考查直线与圆锥曲线的位置关系,综合性强,难度较大@思路……(1)先利用已知条件得到a,bc的关系,并求值,可得椭圆的标准方程;(2)联立直线方程与椭圆方程,利用根与系数的关系及和两条直线对称的条件,求出y轴上存在的定点√3 4=1答案……(1)设椭圆的半焦距为c,由已知可得{c-1.(3分)a2=b2 c2解得c=1,a=2,即b2=3,所以椭圆C的标准方程为 2=1.(5分)(2)假设存在这样的点M,设M(0,1),直线l:y=kx 13x2 4y2=12联立消去y,得(3 4k2)x2 8kx-8=0,△=96(2k2 1)>0.设A(x1,y1),B(x2,y2),



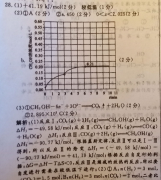
16.(15分)(1)CaC2 2H2b亠ca(OH)2 C2i2↑(2分)(2)除去乙炔气体中混有的H2S、PH3等杂质(2分)(3)1,2,3,1,2,2,4(2分)10y(3分)(5)(2分)6在E装置后再接一个盛有碱石灰的干燥管;向D中通入过量的乙炔,直至酸性KMnO4溶液完全褪色,再测定D及E装置总质量的增加量(4分,各2分)【解析】(1实验室制取乙炔的化学方程式为CaC2 2H2O→Ca(OH)2 C2H2↑。(2)用电石制备的乙炔气体可能含有H2S、PH3等杂质,可以用CuSO4溶液除去。(3)C2H2被KMnO4氧化为CO2,根据得失电子守恒配平方程式(4)根据题意,D、E装置的增重为乙炔的质量,根据关系式:5FeSO4~KMnO4可知,与FeSO反应的KMO的物质的量为5mo,与乙炔反应的KMnO4的物质的量为(x-÷)mol,则乙炔的物质的量为×(x一)mol,乙炔的相对分子质量(5)A装置中产生的气体直接通入酸性KMnO4溶液中,杂质气体也被吸收,会产生误差;乙炔气流太快,通过KMnO4溶液时未被吸收,不影响结果;将E装置换成盛有浓硫酸的洗气瓶,则CO2不能被吸收,会产生误差(6)本实验存在的不足:不能防止空气中水蒸气和二氧化碳对实验的干扰;实验操作较为复杂,两次定量反应也会带来误差。据此进行改进在装置后再接一个盛有碱石灰的于燥管;向D中通入过量的乙炔,直至酸性KMnO4溶液完全褪色,再测定D及E装置总质量的增加量。

以上就是2022英语周报高二34期答案,更多英语周报答案请关注本网站。

 相关文章
相关文章

 栏目最新
栏目最新

 随机推荐
随机推荐 热门标签
热门标签