

0.(10分)(1)500℃、m(NH4Cl)m(菱锰矿粉)=1.10(1分)(2)MCO 2 NH C-MnCI2 2NH↑ COh↑H2O2分)(3)MnO, 2Fe 4Ht-wMn 2Fe 2H2 O(2分(4)Mn2 2HCO" -MnCO, CO:4 H2O2分)5)cO-的水解程度敦大,碳酸铵溶液中c(OH较大,易产生Mn(OH)2沉淀(1分【解析】(1)由图可知,氯化铵焙烧菱锰矿粉的最佳条件是500℃、mCNH4C):m(菱锰矿粉)=1.10,(2)“焙烧”时发生的主要反应的化学方程式为MrCO2 2NH4 Cl-MnCl2 2NH3↑ CO2↑十H2O3)MnO2将Fe氧化为Fe ,反应的离子方程式为MnO 2Fe 4H ?T 2Fe 2H2O(4》“碳化结晶”时,反应的离子方程式为Mn24 2 HCO -MnCO2 CO2↑ H2OO的水解程度较大,碳酸铵溶液中c(OH-)易产生Mn(OH)2沉淀故“碳化结晶”过程中不能用碳酸铵溶液代蒈碳酸氢铵溶液体积为a0.00mL,根据关系式:MnCOLMn(PQ):~(NH)zFe(SO)2可知,n(MC)=n硫酸亚铁铵)=0.2000mol・L-tx0.02L0.004mol,产品的纯度为叫mE则x

1D【解析】因为a)=1# ,所以f(2)=2 A 6=1(1 x 11 2),又1 2 1(1,),所以r(2)∈(,3),由高斯函数的定义可得,函数y=[f(x)]的值域为{0,1,2}.故选D

以上就是2021-2022英语周报高考外研第九期答案,更多英语周报答案请关注本网站。

 相关文章
相关文章



 栏目最新
栏目最新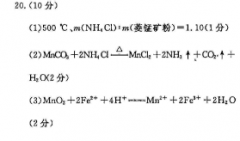

 随机推荐
随机推荐 热门标签
热门标签