

3xx≤23.【解析】(1依题意,得f(x)={2-x1


17.(14分)(1) deane(f(1分)平衡烧瓶和分液漏斗中的压强,便于浓盐酸滴下(2分)(2)16H 2MnO 10C--2Mn2 5Cl2↑ 8H2O(2分)(3)氯化锌发生水解生成Zn(OH)2,Zn(OH)2受热分解生成ZnO(2分,其他合理答案也给分)(4)碱石灰(1分)吸收多余的氯气和HCl,防止污染空气;防止空气中的水蒸气进入装置A(2分)(5)①100mL容量瓶、胶头滴管(2分)680②―%(2分)【解析】(1)装置D制备氯气,进入装置A前,Cl2需要干燥,但Cl2中的HCl杂质不需要除掉,装置C用于处理尾气,故装置的连接顺序为 hecabe(f);装置D中橡皮管的作用为平衡烧瓶和分液漏斗中的压强,便于浓盐酸滴下(2)装置D中反应的离子方程式为16H 2MnO 10C-2Mn2 5Cl2↑ 8H2O(3)气体中有水蒸气杂质时,会导致氯化锌发生水解生成Zn(OH)2,Zn(OH)2受热分解生成ZnO(4)碱石灰不仅可以吸收尾气,同时还能防止空气中的水蒸气进入装置A(5)①配制100 mL Zncl2溶液需要用到的玻璃仪器有量筒、烧杯、玻璃棒、100mL容量瓶、胶头滴管,②根据关系式:ZnCh2~Zn2 ~EDTA可知,ag试样中n(ZnO2)=bmoL×12.50×10-3L.×100ml=25.00m0.05bmol氯化锌的质量分数为0.05mol×136g:mol-1×100%=-%

以上就是英语周报七年级新目标2020~2021第8期答案,更多英语周报答案请关注本网站。

 相关文章
相关文章



 栏目最新
栏目最新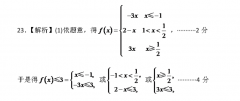

 随机推荐
随机推荐 热门标签
热门标签